*仅供医学专业人士阅读参考铭创配资

解读 女性防治困局——性激素疗法的精准抉择
撰文:Key
2025年阿尔茨海默病协会国际会议(AAIC)于7月27~31日在加拿大多伦多隆重召开。作为认知科学领域最高水平的学术盛会,本届会议吸引了全球顶尖学者的积极参与。来自美国亚利桑那大学的Roberta Diaz Brinton教授会上报告了其团队在性激素疗法与阿尔茨海默病防治领域的最新研究进展。这项从分子机制到临床转化层面的开创性研究,为深入理解女性阿尔茨海默病的特异性发病机制及精准防治策略提供了重要科学依据,本文将梳理会议精彩内容,以饕读者。
女性阿尔茨海默病现状:被忽视的性别差异
首先,Roberta Diaz Brinton教授指出,阿尔茨海默病(AD)是一种以进行性认知功能减退为主要临床表现的神经退行性疾病,其特征性病理改变包括β-淀粉样蛋白沉积形成的老年斑和过度磷酸化tau蛋白构成的神经原纤维缠结。作为痴呆症最常见的类型,该病约占所有痴呆病例的60~70%,全球患病人数已超过5500万且呈快速增长趋势。
流行病学研究显示AD存在显著的性别差异特征,女性患者占到了总患者数的2/3,这一数据背后隐藏着复杂的生物学机制。其中载脂蛋白E(ApoE)ε4基因在其中扮演了重要角色,它对女性,尤其是携带单个ApoE ε4等位基因的杂合子女性患病风险的影响更为显著[1]。此外,围绝经期做为女性生命中的特殊过渡时期,成为了加速衰老的关键节点,而衰老恰恰是AD最重要的风险因素。有证据表明[2],女性在围绝经期阶段可能就已经开始出现与AD相关的病变(图1),这无疑敲响了女性脑健康的警钟。女性不仅患病率更高且疾病进展更快,这一现象促使研究者开始关注性激素在AD发生发展中的潜在调控作用。
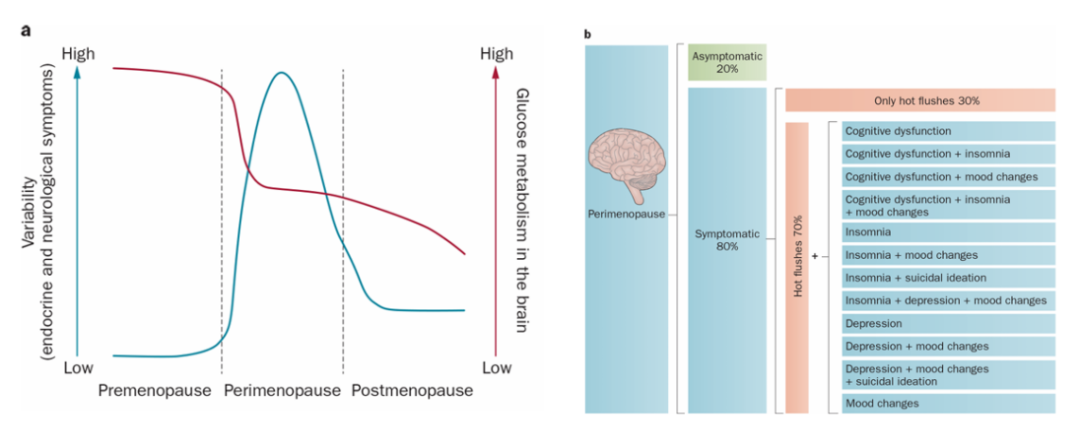
图1 围绝经期至绝经期是女性脑健康的过渡阶段[2]
多学科探究:揭示性激素与AD的深层联系铭创配资
为了深入探究性激素、孕激素以及绝经激素治疗(MHT)对AD相关神经机制及病程进展的影响,Roberta Diaz Brinton教授研究团队采用了分子生物学、细胞生物学等多学科交叉方法,系统揭示了性激素在神经—内分泌—免疫网络中的关键调节作用。其研究结果不仅加深了对雌激素在神经系统中多重作用的理解,也为MHT在AD预防与治疗中的潜在应用提供了理论基础。
雌激素的神经保护作用及其缺失带来的后果
既往大量基础研究表明,雌激素在维持大脑健康方面具有重要的神经保护作用。雌激素能够显著促进大脑葡萄糖代谢,为神经元提供充足而稳定的能量支持;通过增强线粒体功能,提高神经细胞的能量转换效率,从而促进腺苷三磷酸(ATP)的合成,满足中枢神经系统对高能量的持续需求。此外,雌激素还具有调节神经免疫反应、维持神经—免疫平衡的能力,有助于抑制神经炎症过程,降低神经毒性反应的发生率,从而在多层次上保护神经系统的结构与功能完整性。
然而,随着女性进入围绝经期,雌激素水平显著下降,这种内分泌变化会打破原有的神经—内分泌—免疫稳态。研究显示[2],雌激素的缺失会诱发一系列代偿性适应反应,包括神经系统由以葡萄糖为主要能量来源的代谢模式向以酮体或脂肪酸为替代能量的模式转变(图2)。虽然这种代谢重编程在短期内可能具有一定适应意义,但长期而言却可能导致能量供应效率降低、神经元功能受损,进而引发与阿尔茨海默病发病机制密切相关的病理改变,如线粒体功能障碍、神经元突触传递异常、β-淀粉样蛋白沉积及神经炎症激活等。
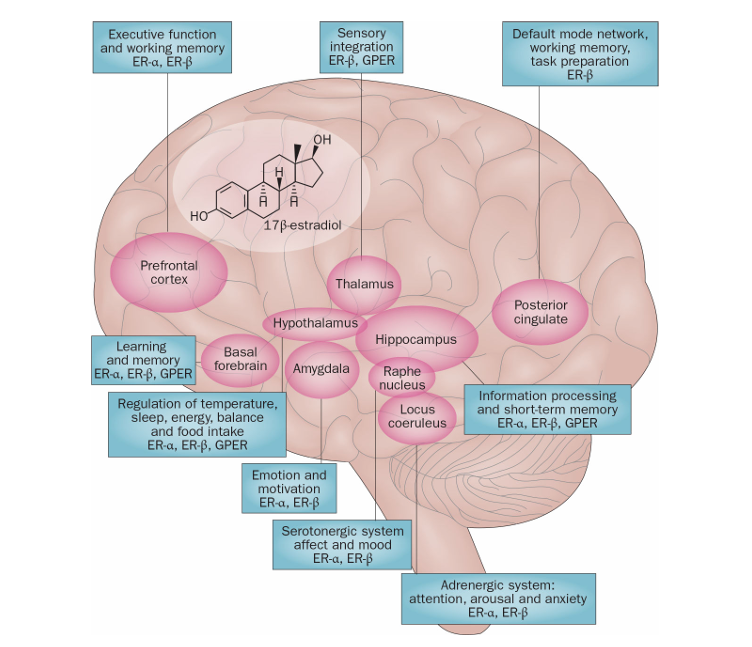
图 2 围绝经期过渡期间性激素对神经系统功能产生的影响[2]
雌激素替代治疗与MHT的效果差异性
在临床前动物模型和细胞水平的研究中,雌激素替代治疗显示出能够有效阻断能量代谢模式的不良转变,维持神经细胞对葡萄糖的敏感性与利用能力,并显著减少神经退行性病变的发生,从而为MHT在AD一级预防中的潜在价值提供了生物学依据。而针对具有明显围绝经期症状的女性实施MHT,可显著降低其罹患AD的风险。
然而,在临床实践中,MHT的治疗效果却表现出高度的个体差异性。观察性研究与随机对照临床试验(RCT)在不同人群中所得出的结果存在明显不一致。例如,对于无明显围绝经期症状的女性,部分研究提示MHT可能无显著益处,甚至可能存在潜在的风险;而另一些研究则显示其对认知功能仍有一定程度的保护作用。这种现象提示MHT的疗效受到多重因素的影响,如使用时机、激素类型与剂量、个体激素受体表达谱、基础代谢状态以及是否存在基因易感因素等。
精准治疗——女性脑健康的关键铭创配资
Roberta Diaz Brinton教授表示,当前普遍认为,MHT的实施需要基于“个体化干预”原则,精准评估目标人群的风险—收益比。尤其是把握“关键时间窗”理论,即雌激素替代治疗可能仅在围绝经期早期启动时才具有神经保护效应,若延迟至神经退行性过程已启动的阶段,反而可能产生负面影响[3]。
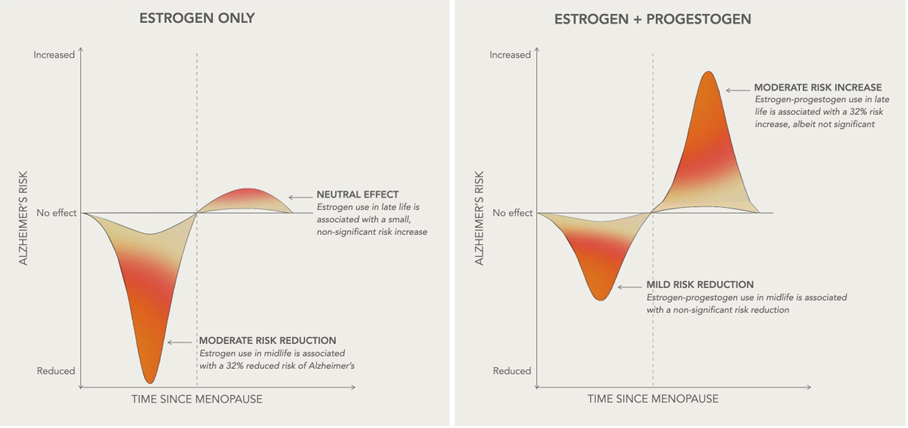
图3 MHT疗法的时机选择至关重要[3]
在围绝经期早期因典型症状而启动MHT,有助于维持认知功能并降低AD的发病风险。这一益处主要归因于围绝经期初期机体对激素水平变化的高度敏感性,在这一阶段及时进行雌激素补充,有望有效调节大脑的代谢与神经功能,从而维持认知健康和神经系统稳态。相较之下,在围绝经期结束较长时间后再启动MHT,其临床效果则可能受到限制,甚至存在轻度增加疾病风险的可能。因为随时间推移,机体的内分泌环境、神经功能状态及代谢模式均已发生显著改变,此时外源性激素可能难以逆转既有的病理过程,部分个体甚至可能出现不良反应或治疗获益有限。
此外,MHT药物的具体配方,尤其是孕激素的种类与剂量,也在很大程度上影响其对神经系统的保护作用。不同类型的孕激素对中枢神经系统的作用机制存在显著差异,其中某些天然或类似天然的孕激素可能与雌激素协同发挥神经保护效应,有助于维持神经元活性与突触可塑性;而部分合成型孕激素则可能对雌激素的有益作用产生拮抗,甚至诱发神经毒性反应。Roberta Diaz Brinton教授强调,在制定MHT方案时,应充分考虑个体的生理状态、激素受体表达特征及认知风险水平,合理选择激素种类与剂量,以实现最大化的治疗收益并降低潜在风险。
护脑还是防癌?破解激素治疗的两难困局
Roberta Diaz Brinton教授介绍,MHT在更年期早期启动,可维持脑代谢与功能稳态,但无法逆转已发生的退行性病变[4]。此外,尽管雌激素具有显著的神经保护作用,但约80%的女性因担心乳腺癌风险而拒绝激素治疗。然而,大脑健康的维持离不开对乳腺安全问题的有效解决。研究发现,雌激素受体β(ERβ)选择性植物雌激素(PhytoSERM)在改善神经功能的同时,能抑制乳腺癌细胞的增殖与迁移。例如,ERβ激活可显著抑制17β-雌二醇诱导的T47D等乳腺癌细胞生长,减少肿瘤形成。目前,ERβ选择性植物雌激素已进入1b/2a期临床试验,初步显示出神经保护与乳腺安全的双重潜力。其从植物中提取、靶向性强、安全性高,有望为女性在认知保护与乳腺健康之间提供新的平衡选择之一[5]。
小结
综上所述,Roberta Diaz Brinton 教授团队的研究为女性AD的防治提供了新的机制认识与干预思路,尤其是在揭示性激素通过调控神经—内分泌—免疫网络影响脑健康方面具有重要意义。ERβ选择性植物雌激素的探索进一步拓展了安全有效的激素替代策略,为兼顾神经保护与乳腺安全提供了可行路径。未来,随着精准医学的发展,有望通过基于个体差异的激素治疗方案,为女性提供更具靶向性和安全性的认知保护手段,从而降低AD的发生风险,切实改善中老年女性的脑健康水平。
参考文献
[1] Hunsberger HC, Pinky PD, Smith W, et al. The role of APOE4 in Alzheimer's disease: strategies for future therapeutic interventions. Neuronal Signal. 2019 Jun;3(2):NS20180203.
[2] Brinton RD, Yao J, Yin F, Mack WJ, Cadenas E. Perimenopause as a neurological transition state. Nat Rev Endocrinol. 2015 Jul;11(7):393-405.
[3] Nerattini M, Jett S, Andy C, et al. Systematic review and meta-analysis of the effects of menopause hormone therapy on risk of Alzheimer's disease and dementia. Front Aging Neurosci. 2023 Oct 23;15:1260427.
[4] Academic Committee of the Korean Society of Menopause. The 2020 Menopausal Hormone Therapy Guidelines. J Menopausal Med. 2020 Aug;26(2):69-98.
[5] Schneider LS, Hernandez G, Zhao L, et al. Safety and feasibility of estrogen receptor-β targeted phytoSERM formulation for menopausal symptoms: phase 1b/2a randomized clinical trial. Menopause. 2019 Aug;26(8):874-884.
责任编辑:梦琳
*\"医学界\"力求所发表内容专业、可靠,但不对内容的准确性做出承诺;请相关各方在采用或以此作为决策依据时另行核查。

微配资提示:文章来自网络,不代表本站观点。